アレロック[よくある医薬品Q&A]
効能又は効果(適応症)
-
アレロックをアトピー性皮膚炎に使用すると適応外使用になりますか?
アトピー性皮膚炎は湿疹・皮膚炎に含まれるとされており、アレロックの適応症である「湿疹・皮膚炎に伴うそう痒」に包括されると考えられます。
【参考】
開発時の皮膚疾患に伴うそう痒に対する臨床試験(成人)ではアレロック錠(普通錠)10mg/日を2週間投与し、アトピー性皮膚炎に対して63.2%(24/38)の最終全般改善度が得られています1)。
また、小児アトピー性皮膚炎患者を対象とした開発治験では、ケトチフェンフマル酸塩を対照とした二重盲検比較試験が行われ、そう痒スコアの治験薬投与前からの変化量(主要評価項目)において、対照薬に劣らない効果(非劣性)が示されています2)。
その他にも、アトピー性皮膚炎患者を対象とした大規模臨床試験では、アレロックのかゆみ再発抑制に関する有用性が報告されています3)。
[参考文献]
1) 西山 茂夫,他 : 臨床医薬 12(8),1615-1640 (1996) [013-346]
2) 川島眞,他:西日本皮膚科,73(3),278-289(2001) [019-735]
3) 川島眞,他:臨床皮膚科,60(8),661-667 (2006) [017-268]2025年10月更新
MA-2023-204
用法及び用量(投与法・投与計画)
-
アレロックの1日2回投与で効果が持続しない場合、1日3回投与は可能ですか?
本剤は、朝及び就寝前の1日2回投与で承認を受けているため、1日3回投与は用法及び用量外使用となります。
本剤を1日3回投与した臨床試験は実施しておらず、有効性や安全性は確立していません。
1日2回投与で効果が不足する場合には、用法及び用量に従って投与回数は1日2回のままとし、1回の投与量を増量する方が好ましいと思われます。
なお、小児においては増量時の安全性は確認されておらず、適宜増減が認められていません。2025年10月更新
MA-2023-204 -
アレロック錠2.5、OD錠2.5を小児に使用することはできますか?
7歳以上の小児に関しては、錠剤・OD錠とも用量が1回5mg(1日2回)で承認されているため、2.5mg製剤を1回2錠服用することは可能です。
2歳以上7歳未満の小児に関しては、錠剤・OD錠は臨床試験を実施しておらず、用法及び用量は設定されていません。2025年10月更新
MA-2023-204
特殊患者への投与
-
アレロックを腎機能低下患者に対して投与する際の投与量の目安はありますか?
腎機能低下患者へ投与する際には、低用量から投与を開始し、患者の臨床所見・臨床検査値の変動を十分に観察しながら慎重に投与することが望まれます。
アレロックは腎排泄型薬剤です。
腎機能低下患者に対して本剤の反復投与時の血中動態並びに安全性、臨床効果を検討した報告は無く、投与方法は確立していません。
成人の腎機能低下患者に単回投与した際に、血中濃度が上昇する事が確認されています1)。
[参考文献]
1) 越川昭三,他:腎と透析,42(1), 107-114 (1997) [013-356]
2025年10月更新
MA-2023-204 -
アレロックは緑内障を合併している患者に投与できますか?
添付文書中には、注意を喚起する記載はなく、緑内障患者にアレロックを投与することは可能であると考えます。しかし、本剤の薬理作用には抗コリン作用がごくわずかですが認められており、安全性を考慮すると使用に際しては経過観察を十分に行うことを推奨します。
【参考】
ラット及びモルモットの組織を用いたヒスタミンH1、ムスカリン、セロトニン5-HT2などの各受容体に対する結合親和性を検討した報告1)では、アレロックの抗コリン作用はその抗ヒスタミン作用と比べて弱いことが示されています。しかし、全く作用しない訳ではなく、モルモット摘出回腸を用いたin vitro試験において、ごく弱いながらも抗コリン作用を示す(IC50値1.6×10-4M)ことが確認されています2)。
[参考文献]
1) 野中裕美,他:薬理と臨床,5(10),1817-1824 (1995) [013-361]
2) 石井秀衛,他 : 薬理と臨床 5(12),2155-2174 (1995) [013-358]2025年10月更新
MA-2023-204 -
アレロックを透析患者に対して投与する際の投与量の目安はありますか?
血液透析患者に対する投与方法は確立していません。
血液透析患者へ投与する際には、低用量から投与を開始し、患者の臨床所見・臨床検査値の変動を十分に観察しながら慎重に投与することが望まれます。
アレロックは腎排泄型薬剤です。
血液透析患者(成人)に投与した際、健康成人と比較して血中濃度の上昇が認められました1)。また透析日と非透析日でほとんど差は認められなかったことから透析性はあまり高く無いと思われます。
[参考文献]
1) 越川昭三,他 : 腎と透析 42(1), 107-114 (1997) [013-356]2025年10月更新
MA-2023-204 -
アレロックは前立腺肥大を合併している患者に投与できますか?
添付文書中に注意を喚起する記載はなく、前立腺肥大患者にアレロックを投与することは可能であると考えます。しかし、本剤の薬理作用には抗コリン作用がごくわずかですが認められており、排尿困難・頻尿等の報告もあることから、安全性を考慮すると使用に際しては経過観察を十分に行うことを推奨します。
【参考】
ラット及びモルモットの組織を用いたヒスタミンH1、ムスカリン、セロトニン5-HT2などの各受容体に対する結合親和性を検討した報告1)では、アレロックの抗コリン作用はその抗ヒスタミン作用と比べて弱いことが示されています。しかし、全く作用しない訳ではなく、モルモット摘出回腸を用いたin vitro試験において、ごく弱いながらも抗コリン作用を示す(IC50値1.6×10-4M)ことが確認されています2)。
[参考文献]
1) 野中裕美,他:薬理と臨床,5(10),1817-1824 (1995) [013-361]
2) 石井秀衛,他 : 薬理と臨床 5(12),2155-2174 (1995) [013-358]2025年10月更新
MA-2023-204 -
アレロックはてんかんを合併している患者や熱性けいれんの既往歴のある患者に投与できますか?
本剤の添付文書に注意等の設定はされていませんが、抗ヒスタミン作用を主作用とすることから、てんかん患者及び熱性けいれんの既往歴のある患者への投与に際しては十分な経過観察が重要となります。
ヒスタミンは、脳内において痙攣に対し抑制的に作用すると考えられています1,2)。
このため、抗ヒスタミン作用を有する薬剤をてんかん患者に投与すると痙攣発作が誘発される可能性があります。
[参考文献]
1) 横山 浩之 : 臨床脳波 39(1), 13-17 (1997) [015-794]
2) 飯沼一宇 : アレルギー・免疫 12(2), 286-291 (2005) [017-254]2025年10月更新
MA-2023-204
副作用・安全性
-
アレロックを過量投与(誤飲)したときに予測される副作用および処置法はありますか?
アレロックの用量依存的に生じる副作用として眠気及び倦怠感等の発現が考えられます。
成人での第I相試験1)において、オロパタジン塩酸塩80mgを単回投与した結果、6例中4例に眠気、1例に倦怠感(眠気併発)、1例に頭がボーッとする感じが発現したが、血圧、脈拍数、体温に特記すべき所見は認められておりません。
その他の臨床症状が認められた際には、症状に応じた対症療法を行うことになります。
誤飲の際は、まず「年齢」、「服用した量」、「どれ位前に服用したのか」、「現在の状態(意識状態・呼吸・血圧など)」を確認します。
対応としては以下のようなことが考えられます。
1.通常は経過観察をしてください。
アレロックは服用後1時間程度でTmaxに達する薬剤です。何かしらの症状が出る際はこの時期に発現する可能性が高いと思われます。服用後どれくらいの時間が経過しているかを確認してください。
時間が経過していれば、その後特に大きな問題になる事は考え難いものの、可能であれば1日程度入院にて経過観察をお願いします。また通常と様子が異なるようであれば、医師の立ちあいのもと対症療法を実施してください。
2.アレロックは腎排泄型薬剤のため、必要に応じて体外への薬物排泄を促すように輸液等で補液を実施してください。
なお、アレロックは血液透析によって1割程度しか除去されませんので2)、血液透析による除去は期待できません。
[参考文献]
1) 角尾道夫,他 : 基礎と臨床 29(16),4129-4147 (1995) [013-372]
2) 越川昭三,他:腎と透析,42,(1),107-114 (1997) [013-356]2025年10月更新
MA-2023-204 -
アレロックは肝代謝が少ないにもかかわらず、肝機能障害等が発現するのはどうしてですか?
アレロックによる肝機能障害の発現機序は不明です。
なお、本剤が主に腎排泄によって体内から消失する薬剤であるため、肝機能に直接影響を与えるとは考えにくいこと、薬物リンパ球刺激試験(DLST)で陽性が認められた症例があることから、アレルギー性の機序による発現が示唆されています。
アレロックは発売当初、AST上昇、ALT上昇等の臨床検査値異常が添付文書に記載されていましたが、市販後にこれらの記載からは予測できない症例が6例集積されたため、2002年12月に重大な副作用として「肝機能障害、黄疸(頻度不明)」を追記しました。
その後、本剤との関連性が否定できない「劇症肝炎」が2例集積されたため、2011年4月に「劇症肝炎」を追記しています。2025年10月更新
MA-2023-204 -
アレロックによる眠気の発現頻度や程度はどのようなものですか?また、その処置はどうすればよいですか?
臨床開発治験時および使用成績調査・特別調査(成人)における眠気の発現頻度は7.0%(674例/9620例中)でした。眠気の程度は臨床開発治験時の眠気発現症例203例を解析すると53.2%(108例/203例中)が「軽度」でした。
眠気発現症例において減量、休薬・中止等の処置を必要としなかった症例は64.5%(131例/203例中)で、残りの症例も減量及び休薬・中止の措置により軽快又は回復しています。
また、7歳以上の小児を対象とした普通錠、OD錠の臨床試験及び特定使用成績調査において、3451例中142件(4.1%)に眠気の副作用が発現しました。(「重篤」と判定された症例はありませんでした)。多くは本剤投与開始直後に発現し、投与を中止することなく回復しており、長期投与による症状の重症化などは認められませんでした。2025年10月更新
MA-2023-204
妊娠・授乳への影響
-
アレロックは妊婦へ投与できますか?
動物実験(ラット、ウサギ)1-3)では催奇形性は認められていませんが、妊婦を対象とした試験は実施していないことから、添付文書9.特定の背景を有する患者に関する注意「9.5 妊婦」に、「治療上の有用性が危険性を上回ると判断される場合にのみ投与すること」と記載しています。
[参考文献]
1) 納屋聖人,他 : 基礎と臨床 29(19), 4803-4814 (1995) [013-365]
2) 納屋聖人,他 : 基礎と臨床 29(19), 4815-4839 (1995) [013-364]
3) 納屋聖人,他 : 基礎と臨床 29(19), 4841-4852 (1995) [013-363]2025年10月更新
MA-2023-204 -
アレロックは授乳婦へ投与できますか?
治療上の有益性及び母乳栄養の有益性を考慮し、授乳の継続又は中止を検討してください。動物実験で乳汁中への移行が認められており1)ヒトにおいても母乳中へ移行する可能性が考えられます。
[参考文献]
1) 大石孝義,他:薬物動態,10(5),707-721(1995) [013-375]2025年10月更新
MA-2023-204 -
授乳婦がアレロックを服用している場合、服用中止後どの程度経過したら授乳してもよいですか?
アレロック(普通錠)の反復投与時の体内動態の結果より推測すると、万全を期する意味では本剤服用中止後5-7日程度は授乳を避けたほうが良いと考えられます。
本剤10mg錠を健康成人男子に反復経口投与した場合のT1/2は11.47時間でした。投与中止後72時間の血漿中濃度は1ng/mL以下の値を示しており、わずかですが血中に認められています1)。
【補足】
動物試験にて乳汁移行が認められています2)。授乳期のラットに本剤1mg/kgを経口投与した場合、本剤の乳汁中未変化体濃度は、投与後0.25-24時間では、血漿中未変化体濃度の0.36-1.97倍でした。また、乳汁中未変化体AUC0-24(844.6 ng・hr/mL)は、血漿中未変化体のAUC0-24(817.2 ng・hr/mL)とほぼ同等でした。
従って、服用中止後から授乳までにwash outの期間を設ける必要があると考えられます。
[参考文献]
1) 大石孝義,他:薬物動態,10(5),707-721 (1995) [013-375]
2) 角尾道夫,他:基礎と臨床,29(16),4129-4147 (1995) [013-372]2025年10月更新
MA-2023-204 -
男性がアレロックを服薬している場合、妊娠成立や胎児への影響はありますか?
アレロックの精子に対するヒトでの影響、および男性生殖器機能に対する影響については、現在のところ検討はされておりません。
アレロックの生殖発生毒性試験(ラットを用いた妊娠前及び妊娠初期投与)1)では、次世代の発生に及ぼす影響は認められず、胎児死亡率、生胎児率、胎児体重には対照群との間に差はみられず、外表異常の発生増加も認められていません。
受胎率については、雌雄ともに統計学的に有意ではないものの、400mg/kg群で低下傾向がうかがわれました。
[参考文献]
1) 納屋聖人,他:基礎と臨床,29 (19),4803-4814 (1995) [013-365]2025年10月更新
MA-2023-204
配合変化・安定性
-
アレロック錠を粉砕したときの安定性データはありますか?
以下のデータを取得しています(2.5mg錠での検討)。
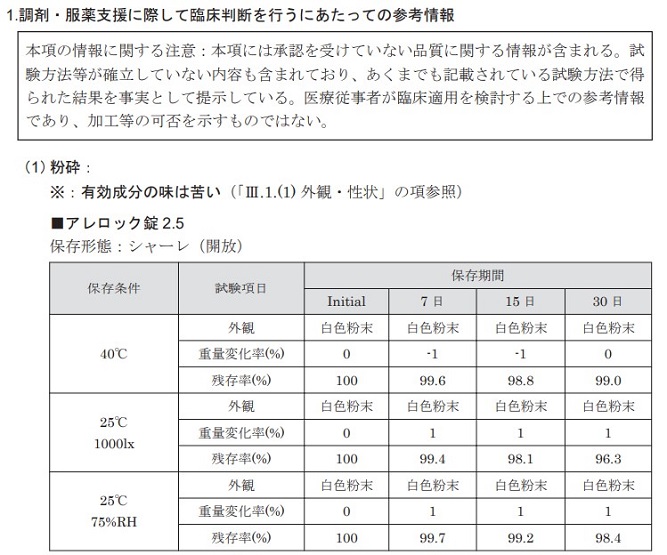
注意:承認を受けていない用法に関する情報が含まれます。試験方法等が確立していない内容も含まれており、あくまでも記載されている試験方法で得られた結果を事実として提示するものです。医療従事者が臨床適用を検討する上での参考情報であって、加工等の可否を示すものではありません。なお、粉砕・半割した薬剤の体内動態、有効性、安全性は検討していません。2025年10月更新
MA-2023-204 -
アレロックOD錠を粉砕したときの安定性データはありますか?
以下のデータを取得しています(OD5mg錠での検討)。
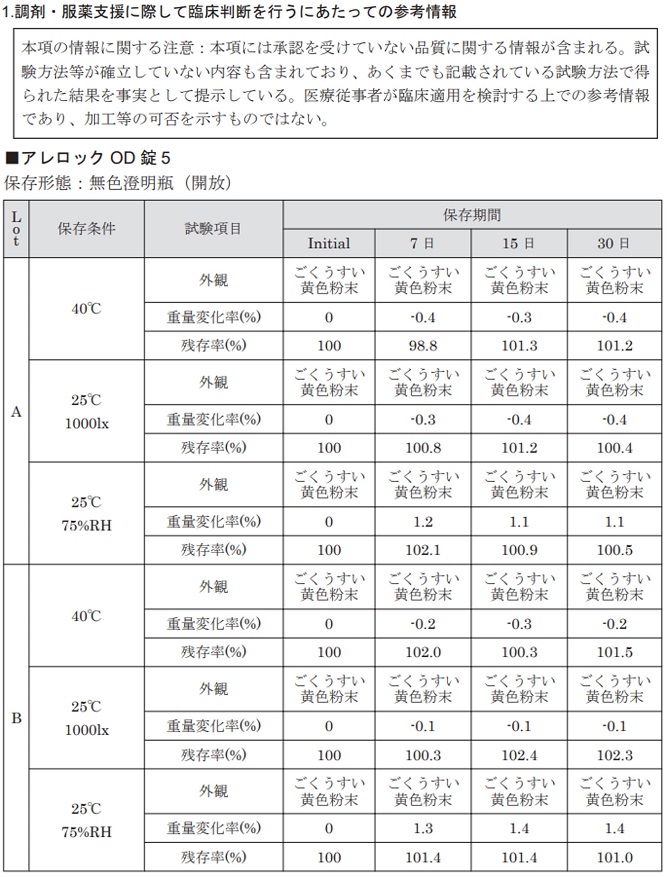
注意:承認を受けていない用法に関する情報が含まれます。試験方法等が確立していない内容も含まれており、あくまでも記載されている試験方法で得られた結果を事実として提示するものです。医療従事者が臨床適用を検討する上での参考情報であって、加工等の可否を示すものではありません。なお、粉砕・半割した薬剤の体内動態、有効性、安全性は検討していません。2025年10月更新
MA-2023-204
製剤学的事項
-
OD錠の味は?
パイナップル風味です。
2025年10月更新
MA-2023-204
薬理作用(作用機序)
-
アレロックを服薬中に予防接種(ワクチン投与)を受けた場合、予防接種の効果に影響はありますか?
一般的に抗アレルギー薬(ステロイド以外)は、予防接種(ワクチン投与)の効果へは影響しないと考えられています1)。
アレロック服用中に予防接種を実施し影響を検討された報告はありませんが、開発時にIgE抗体に及ぼす影響についてマウスを用いて検討したところ、IgE抗体産生に影響しないことが確認されています。今のところ、本剤の投与は抗体産生・免疫獲得に影響を与えないと考えられています。
[参考文献]
1) 永淵正法,他 : 日本医事新報 No.3776,111 (1996) [014-406]2025年10月更新
MA-2023-204






